開 発 製 品|医療分野
レーザー、衝撃波を応用した、「診断装置」「手術装置」「治療装置」を開発しています。
パルスジェットメス(PJM:下垂体腫瘍)
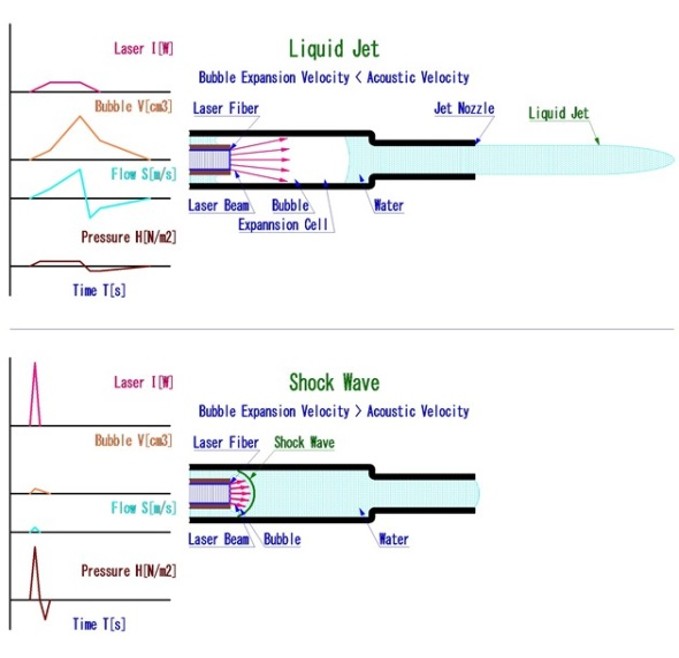
水に吸収率の高い波長のレーザーを水中照射すると、プラズマ気泡が生成・膨張し、水の移動速度よりも遅い速度で膨張する場合、水が押し出され、ノズルを設けると液体ジェットが生成されます。
レーザー誘発液体ジェットは、水の移動速度よりも速い速度で膨張する場合、水が移動できず気泡周辺部に高圧力部が生成されます。(レーザー誘導衝撃波)
レーザー誘発液体ジェットは「数十メートル/秒の」初速を持ち、生体組織に照射すると、組織弾性率の差で破砕と温存が明確に生じさせることができます。「パルスジェットメス」はレーザー誘発液体ジェットを用いた手術装置です。
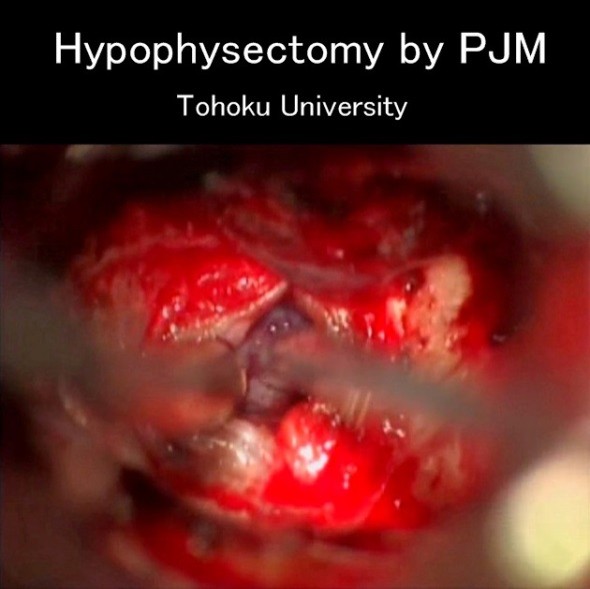
脳に照射した場合、脳組織が破砕され、血管が温存されます。視野が狭く出血が許されない、「経蝶骨的下垂体腫瘍切除術」に適用し、効果を上げました。(多施設臨床試験)
「最大限の病変摘出と機能温存を両立するパルスジェットメスの開発」が「平成22年度課題解決型医療機器の開発・改良に向けた病院・企業間の連携支援事業」 (H23実施;経済産業省)に採択されました。
■ 第1次共同開発機関:東北大学脳神経外科、東北大学流体科学研究所、東京電機大学、
産業技術総合研究所
■ 第2次共同開発機関:東京科学大学神経外科、東京電機大学、東北大学脳神経外科
眼底光学干渉断層計(OCT)
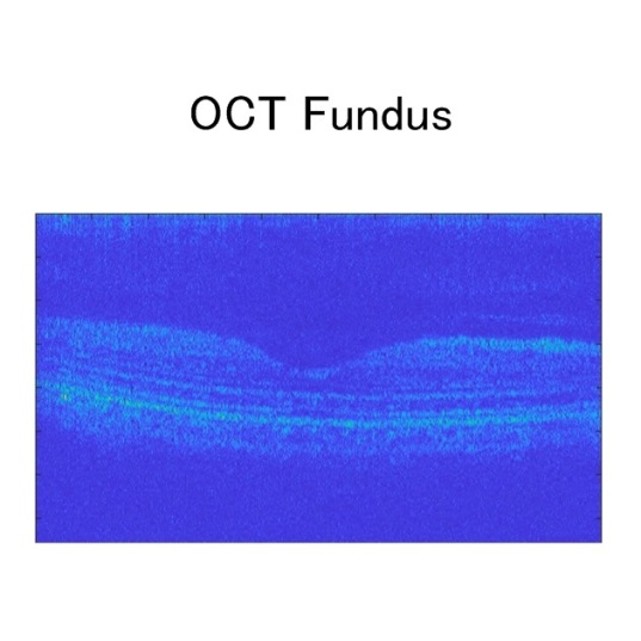
失明の要因である「緑内障」「加齢黄斑変性症」の早期診断を脈絡膜の健全性で評価して、早期治療に繋げ、失明率を低下させる。脈絡膜の健全性を評価するには微細な脈絡膜を捉え、水平面での表示が必要です。
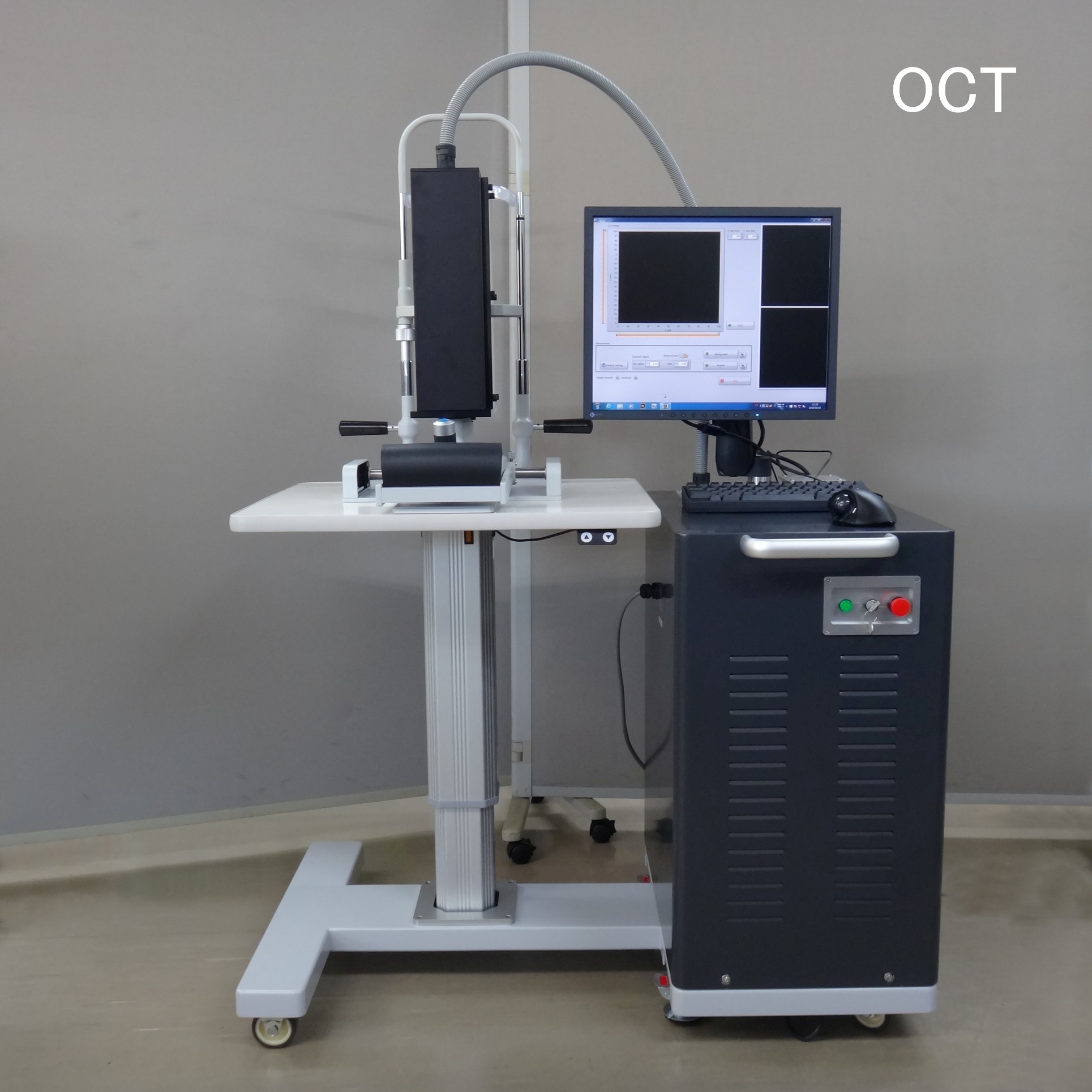
眼底光学干渉断層計は、眼底の断層撮影に光干渉断層撮影法(OCT: Optical Coherent Tomography)を用います。
眼底各点に広帯域光源光を照射して、後方散乱光を参照光と干渉させ捉え、フーリエ変換により眼底各点の断層データに変換し、更にスキャナーでX-Yに展開し、得られたデータを3次元で再構成します。
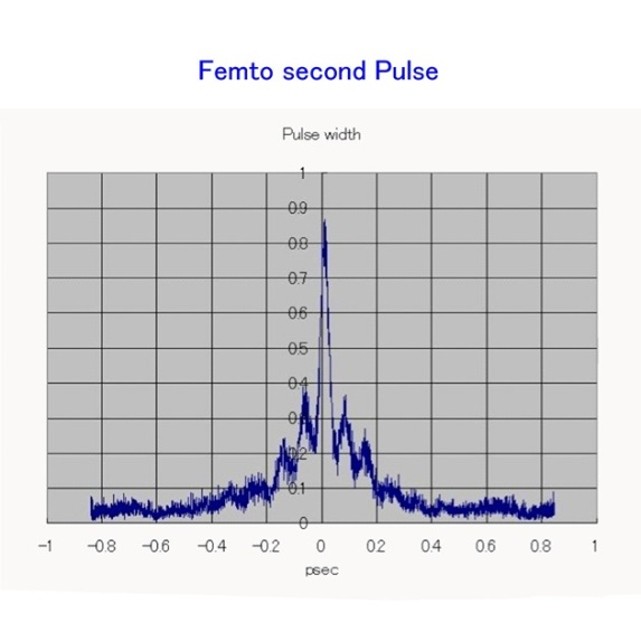
本装置の特徴は、広帯域光源にフェムト秒ファイバーレーザー起源の「スーパーコンティニュアム光源(SC)」を用いる点にあります。SCは起源となるファイバーレーザーがモードロック発振であるため、各モード間の位相差が安定しており、各モードの干渉性が良いです。またフェムト秒パルスで高ピーク出力のため、ファイバー内での非線形現象により波長幅が広帯域に拡がります。これらの特性から光学干渉断層計に適しています。
「特殊レーザーを用いた高分解能・高速・高感度OCT装置」課題が「平成25年度課題解決型医療機器等開発事業」(経済産業省)、「平成26年度~平成27年度医工連携事業化推進事業」(AMED)に採択されました。
共同開発機関:埼玉医科大学眼科システムがこの画像を描出できる可能性があります。
2013年より開発を開始し、2015年に試作機が完成しましたが、眼底後方散乱光強度の不足、分光カメラの性能(低感度・高ノイズ)の問題から、波長帯の変更、分光カメラの換装を課題とし、現在は自社開発を継続しています。
■ 共同開発機関:埼玉医科大学(眼科)、株式会社イナミ
多チャンネルレーザー温熱治療装置
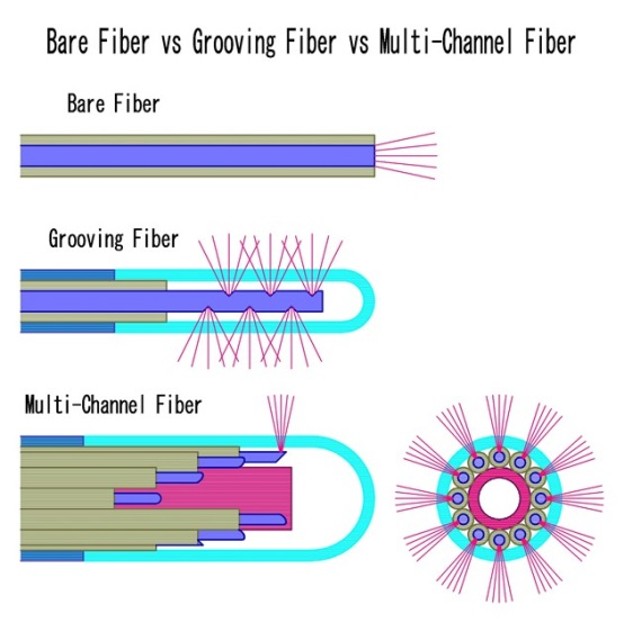
異形状の腫瘍に対して均質に光照射するためには、形状に合わせた光強度分布を生成する必要があります。従来、拡散ファイバーや、照射点が移動する可動ファイバーが用いられていました。
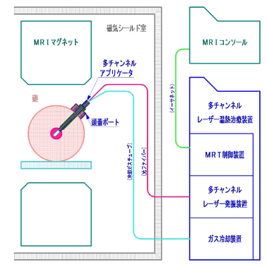
多チャンネルレーザー温熱治療装置は、以下のユニットから構成され、異形状腫瘍のレーザー温熱治療が可能です。
① 照射点の異なる多数のファイバーを組込んだアプリケータ。アプリケータは光ファイ
バーを含めて、全て非磁性体で構成され、MRI電磁場内での使用が可能です。
② 各ファイバーに1対1に接続されたレーザー群。
③ 各レーザーを個別に制御する制御システム。MRT温度情報に基づくレーザー群の制
御にはAIを用います。
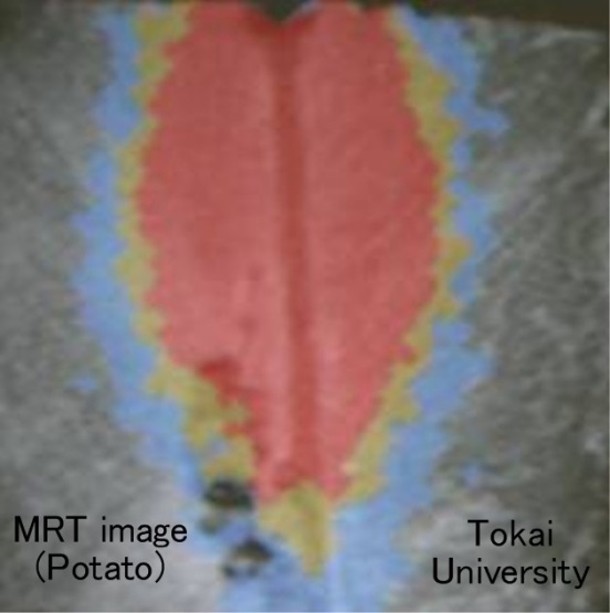
④ 生体内3次元温度分布を計測するMRTシステム。MRTは、MRIで取得した位相情
報から温度へ変換して、3次元温度分布を求めます。
■ 共同開発機関:東海大学脳神経外科、東京電機大学、産業技術総合研究所、
株式会社ミズホ
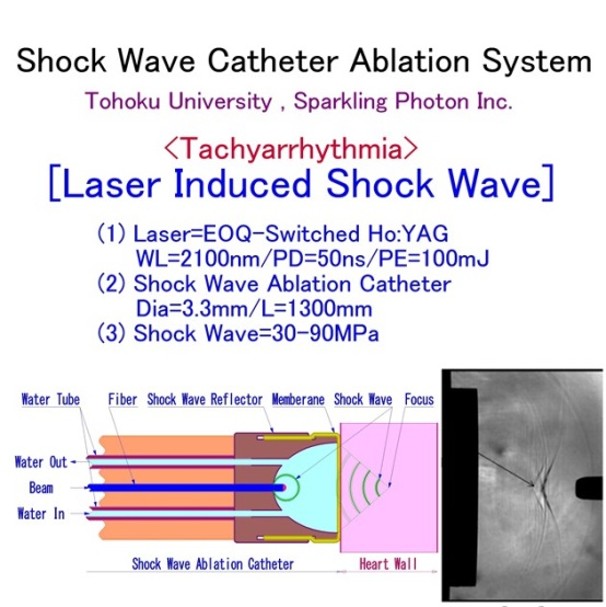
衝撃波カテーテルアブレーションシステム(LSA)
水に吸収性の高い波長のレーザーを水中照射すると、プラズマ気泡が生成・膨張します。
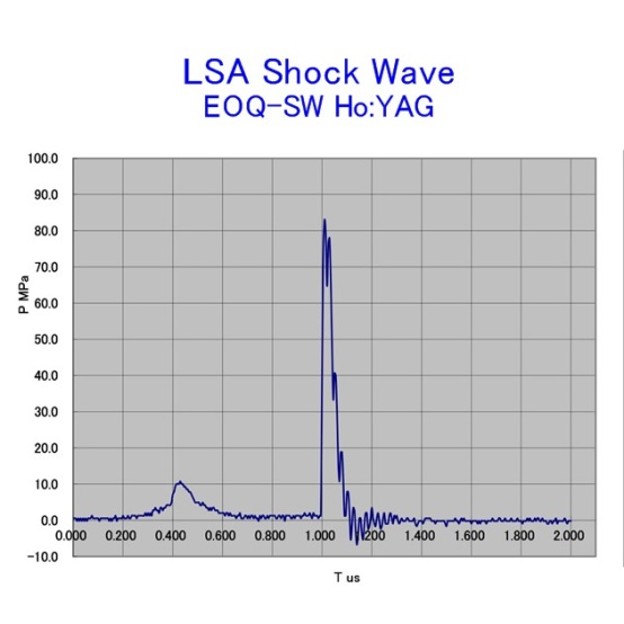
水の移動速度よりも速い速度で膨張する場合、水が移動できず、気泡周辺部に高圧力部が生成される「レーザー誘導衝撃波」が発生します。
(水の移動速度よりも遅い速度で膨張する場合、水が押し出され、ノズルを設けると液体ジェットが生成されます。「レーザー誘発液体ジェット」)
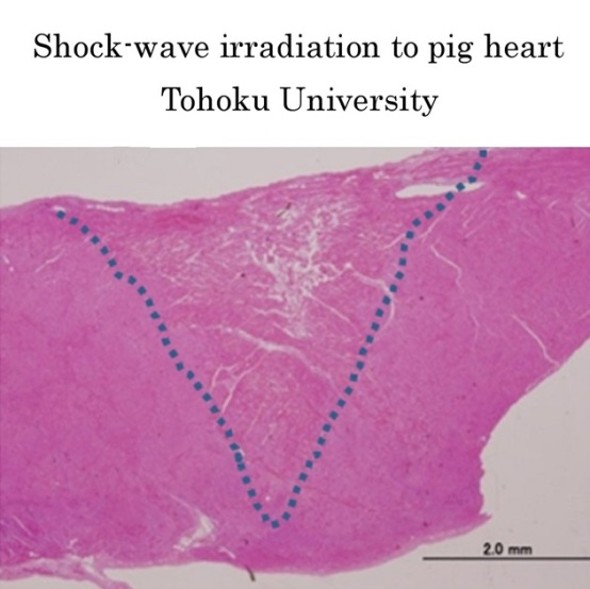
カテーテル先端で衝撃波を発生・収束させ、生体組織に照射すると、収束点で弾性流が発生し、収束点以遠でも組織変性が起きます。(=衝撃波カテーテルアブレーションシステム)
従来のカテーテルアブレーション治療は、不整脈基部周辺組織を高周波電流により熱凝固して、神経の電気的な導通を遮断します。本装置は高周波電流アブレーションを、衝撃波によるアブレーションに置き換えたものです。
高周波電流アブレーションでは、組織表層より進達する熱変性を用いますが、衝撃波アブレーションでは、低温で内部変性を起し、血栓が無い、深深度の治療が可能です。
「衝撃波カテーテルアブレーションシステムの開発」課題は、「平成30年度~令和2年度医療機器開発推進研究事業」「令和3年度橋渡し研究プログラム」 (AMED)に採択されました。またPMDAとの「医療機器戦略相談」において、「治験開始に関して問題なし。」との助言を受けています。
■ 共同開発機関:東北大学循環器内科、東北大学流体科学研究所、
サウンドウェーブイノベーション株式会社